Pixiv - KiraraShss
结构化学基础叁
288 字
1 分钟
结构化学基础叁
约定:本文用加粗标记定义或概念,实验名称由斜体标注。本文中部分图片为网图,侵删。
1. 共价键
共价键的本质是由于原子相互接近时轨道重叠,而重叠的部分通过共享电子使能量降低,从而形成共价键,两个原子间也就有了相互作用力。
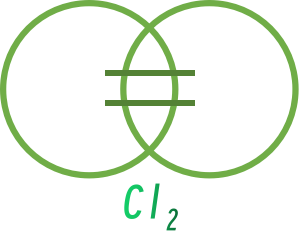
共价键具有饱和性与方向性。
1.1 饱和性
每个原子在形成共价键时,能够提供的未成对电子数和轨道数是一定的,所以每个原子成键的总数或以单键邻接的原子数目就一定。
按照价键理论,元素原子可能形成的共价键数是与原子的价轨道数和价电子数有关,并不受 八隅体的限制。
1.2 方向性
共价键具有方向性。
- 成键时两个轨道“头碰头”地重叠,形成的是 键。如两个 轨道,两个 轨道, 与 轨道,能够形成 键。
- 两个轨道“肩并肩”地重叠,形成的是 键。
unfinished
支持与分享
如果这篇文章对你有帮助,欢迎分享给更多人或赞助支持!
相关文章 智能推荐
1
结构化学基础贰
笔记本 2023-07-15
2
结构化学基础壹
笔记本 2023-07-13
3
速通《乡土中国》
笔记本 2023-08-15
4
Casio991 常数说明
笔记本 2023-08-08
5
社团改名:一种文化心态的反思
展览厅 2025-12-02
随机文章 随机推荐
 无穷大?
无穷大? 











